1968年Friedenstein等发现鼠骨髓中的一群细胞可形成纤维细胞样的克隆,并且能通过体外诱导分化形成骨组织,移植入小鼠皮下后可重建造血微环境。后期科学家发现骨髓中的这些细胞可分化为骨细胞、软骨细胞、脂肪细胞和肌肉细胞。1991年这种来自骨髓的细胞被命名为间充质干细胞(Mesenchymal Stem Cells,MSC)。后来多种不同组织(骨髓、肌肉、脂肪、胎盘、脐带、牙髓等)的前体细胞均被统称为MSC,不同组织的发育过程不同,这些前体细胞属于完全不同的细胞类型。由于这些MSC易于分离扩增,科学家对其开展了规模化培养和临床研究。但是,不同来源的MSC克隆形态、分化潜能、自我更新能力和基因表达谱各异, 这些差异也给MSC产品生产工艺的开发和质量标准的设置等研究带来了挑战。
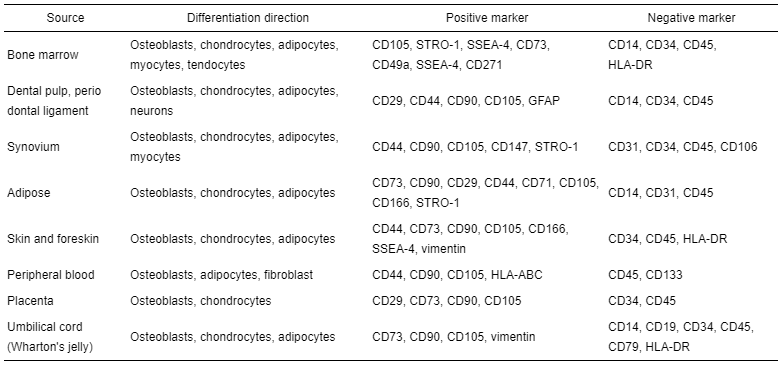
根据ISCT发布的指南,体外扩增的人MSC表达细胞表面标志物CD73、CD105和CD90,缺乏内皮细胞和造血干细胞标志物CD34、CD31和CD45。然而由于MSC可来源于多种组织,对此目前存在争议, 如有研究认为特定阶段胚胎抗原-4 (stage-specific embryonic antigen-4, SSEA-4)、CD146和基质前体抗原-1 (stromal precursor antigen-1, Stro-1)也可以作为间充质干细胞的标志物。各个组织来源的MSC分子标志物表达有所差异,如有研究认为牙周膜源MSC的CD90表达量较其他分子多,而脂肪源MSC的CD105表达量相对多。Stro-1可表达于骨髓和牙髓来源的MSC, 但不能表达在脂肪来源的MSC中。通常来说,脂肪来源的MSC细胞表达高水平的CD49d、CD34和CD54分子, 骨髓来源的MSC表达较高水平的CD106, 同时表达Stro-1、CD105、SSEA-4、CD73、CD49a和CD271等分子, 而脐带来源的MSC不表达CD271分子, 来自胎儿组织的MSC表达部分多能干细胞标志物包括SSEA-3/4和Oct-4 (octamer-binding transcriptional factor-4)等。不同组织来源、不同形态的MSC,也具有显著不同的转录组表达谱和不同的体内分化潜能。(如下表所示)
间充质干细胞通过内分泌/旁分泌系统分泌生物活性因子和外泌体。释放细胞因子、生长因子、抗氧化剂和促血管生成因子的分子,以及刺激细胞增殖和血管生成的分子。 这降低了压力和受损细胞凋亡的反应。 通过调节局部和全身的炎症和免疫反应来修复组织。其主要功能主要包括:
1. 归巢功能。
间充质干细胞具有归巢功能,当身体组织受到某种刺激时,它将会“唤醒”一些正在“休眠”的间充质干细胞,并归巢到损伤部位进行分化,替代损伤的细胞。间充质干细胞能通过不同信号以调控干细胞向目标组织迁移,修复人体损伤、老化的组织和器官。
2. 抗炎作用
它可以减少排斥反应(GvHD),间充质干细胞有先天性免疫原性优势,它可通过直接接触、分泌可溶性因子作用于体内免疫细胞而发挥免疫调节功能;更能趋向定位于发炎部位发挥抗炎作用。
3. 分泌良好的细胞因子
间充质干细胞迁移分化能力强,能分泌多种良好的细胞因子,这些因子可以刺激间充干细胞发挥免疫抑制功能,在短时间内大量生长良好的干细胞以促进受损细胞的存活。
4. 促进血管生成
血管生成是在多种促血管生成因子和抗血管生成因子的平衡调节下进行的,间充质干细胞可以诱导血管的生成及促进血管生成作用,也具有调控造血干细胞的功能,因此间充质干细胞被认为是组织细胞再生的理想细胞。已被用于皮肤缺损、缺血性疾病、神经损伤等临床疾病的治疗。
近年来MSC相关研究取得了很大进展, 尽管人们对其作用机制的研究仍处于初期阶段, MSC对体内环境的适应性及其对多种疾病的潜在治疗能力依旧赋予其期盼的治疗优势。作用机制方面, 目前尚未研究清楚的问题包括: MSC移植后的存活、迁移和归巢机制; MSC与宿主免疫系统的相互作用; 体内增殖、分化和转分化潜力等。目前多数研究初步揭示了MSC对部分疾病的治疗作用, 但大部分均通过MSC自身细胞因子的分泌实现, 并非由细胞本身的作用导致。未来的MSC研究开始聚焦在特定来源MSC的分子标志物的发现,以及MSC分化、转分化、归巢等行为的调控因子的发现上。MSC的临床给药方式、适应症和受试者的选择等显著影响MSC临床试验的结果, 前期MSC临床试验的成功和失败案例也为后续临床治疗方案的制定提供了重要参考依据。生产工艺方面, 细胞分离工艺、培养条件和制剂工艺的开发有许多难点, 包括供者细胞个体化差异带来的不确定性、关键工艺参数的确定、如何保证产品批间一致性等。对于规模化培养工艺, 细胞制备过程细胞癌变的风险也应进行研究确证。质量研究方面, 效价检测、死细胞/杂质残留量的检测等方法的开发具有较大挑战, 细胞分化能力测试需长时间进行细胞诱导培养, 检测周期长。此外, 流式细胞分析等方法的优化和相关方法学验证也是细胞质控所必需的。
目前各国药品评价机构均对干细胞产品的研发和临床应用高度关注。在我国,随着2017年《细胞治疗产品研究与评价技术指导原则(试行)》等文件的出台和实施,相关管理部门将逐步规范和细化细胞治疗产品的技术评价,实现临床急需和创新型细胞产品的快速审评,促进干细胞产业良性、健康和有序的发展。
本篇文章所含内容如果涉及侵权请联系我们及时处理,感谢您的理解!
上一篇: 间充质干细胞外泌体